Proteine
Um eine einwandfreie adhering junction zu generieren, arbeiten eine Reihe von Proteinen zusammen. Dabei gibt es zwei verschiedene Transmembranproteine, die diese junctions ausbilden können: Das calciumabhängige Cadherin sowie das calciumunabhängige Nectin. Auch wenn an beiden Möglichkeiten unterschiedliche weitere Proteine beteiligt sind, ist der Aufbau ähnlich: Extrazellulär bindet das Transmembranprotein (Cadherin oder Nectin) an das gleiche Protein der Nachbarzelle, sodass eine Brücke über den 15-25 nm breiten Interzellulärraum gebildet wird. Intrazellulär verbindet dann ein Ankerprotein das Transmembranprotein mit dem Zytoskeletts, sodass der Komplex stabiler ist. Wenn eine Reihe von diesen Komplexen nebeneinanderliegt, erhält man so eine Art Reißverschlussstruktur.
Im Speziellen ist das Ankerprotein bei Cadherin das Catenin, wobei verschiedene Arten davon mitwirken. Cadherin bindet an β-Catenin oder γ-Catenin (Plakoglobin), welches wiederum an α-Catenin gebunden ist, das an den Aktinfilamenten hängt. Im zweiten Fall bildet Nectin einen Komplex mit dem Ankerprotein Afadin.
Der Unterschied zwischen den Macula adhaerens und Zonula adhaerens besteht darin, dass der Proteinkomplex im ersteren Fall an das Zytokeratin der Intermediärfilamente und im zweiteren Fall an die Aktinfilamente bindet. [1, 2, 3, 4]
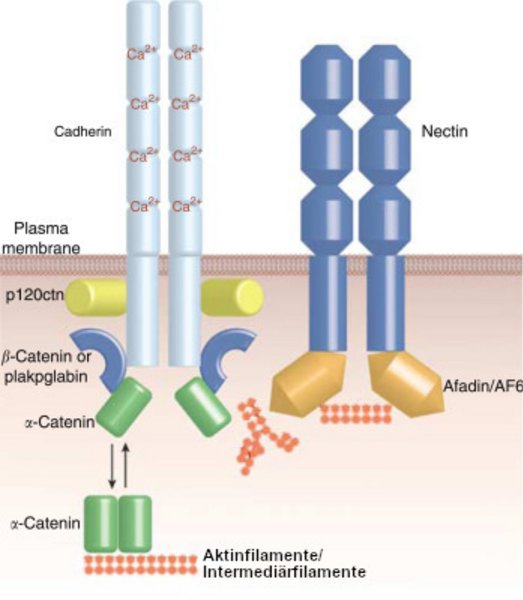
Darstellung einer Plasmembran mit Proteinen einer adhering junction wie sie beispielsweise in Herzmuskel-, Epithel- und Gliazellen sowie in der Retina vorkommt.
(https://ars.els-cdn.com/content/image/1-s2.0-S0022202X15331833-gr1.jpg)
Quellen:
[1] https://www.sciencedirect.com/science/article/pii/S0022202X15331833
[2] https://www.biologie-seite.de/Biologie/Adherens_Junction
 <map name="Map" id="Map"> <area alt="" title="Startseite" href="https://www.uniklinikum-saarland.de/einrichtungen/fachrichtungen/zellbiologie/seminar_zellbiologie_20192020/zell_zell_kontakte/" shape="poly" coords="5,4,89,5,90,22,5,24" /> </map>
<map name="Map" id="Map"> <area alt="" title="Startseite" href="https://www.uniklinikum-saarland.de/einrichtungen/fachrichtungen/zellbiologie/seminar_zellbiologie_20192020/zell_zell_kontakte/" shape="poly" coords="5,4,89,5,90,22,5,24" /> </map>




