Molekularbiologie des Meningeoms
1. Alkalische Phosphatase in Meningeomen
Bei Meningeomen handelt es sich in der Regel um gutartige Tumore, die sich von den Hirnhäuten ableiten. Nur ein kleiner Anteil entwickelt sich zu malignen Formen: einem 'intermediate' Typ oder einem anaplastischen Tumor. Diese Tumore werden nach der WHO Klassifizierung als WHO Grad II bzw. III bezeichnet. Zytogenetisch weisen WHO Grad I Tumore entweder einen normalen Karyotyp oder eine Monosomie bezüglich Chromosom 22 auf. Strukturelle Veränderungen treten unregelmäßig auf mit Ausnahme des Verlustes vom kurzen Arm von Chromosom 1, der einen entscheidenden Schritt bei der Tumorprogression spielt. Aus Vergleichen von histochemischen und zytogenetischen Untersuchungen ergibt sich, dass das Gewebe-unspezifische Alkalische Phosphatase-Gen (auch als liver/bone/kidney Typ bezeichnet), welches auf dem kurzen Arm von Chromosom 1 in der Region 1p36.1-p34 liegt, ein Kandidat für ein Tumorsuppressor-Gen darstellt. Bei der Progression des Meningeoms kommt es zu einer Inaktivierung des Enzyms Alkalische Phosphatase, die von diesem Gen kodiert wird. Allerdings bedeutet der Verlust von einem Chromosom 1 bzw. dem kurzen Arm des Chromosoms, dass noch ein Chromosom 1 in der Zelle vorhanden ist. Immunologisch und histochemisch ist aber weder das Enzym noch eine Enzymaktivität nachweisbar (Niedermayer et al. 1997a). Möglicherweise ist das Alkalische Phosphatase-Gen auf dem verbleibenden Chromosom mutiert, so dass das translatierte Enzym inaktiv ist. Bisherige Analysen ergaben keine Mutationen auf dem Alkalische Phosphatase-Gen (Prowald et al. 2002a).
Bei der Gewebe-unspezifischen Form der Alkalischen Phosphatase kennt man zwei Promotoren. Die translatierten Proteine unterscheiden sich nicht, lediglich in der mRNA ist das erste Exon verschieden (Weiss et al. 1988; Matsuura et al. 1990). Dieser Unterschied ist durch alternatives Splicen bedingt. Das erste Exon wird 1L (L für liver, Leber) bzw. das alternative erste Exon wird 1B (B für bone = Knochen) genannt. In Meningeomen wurde bisher als transkribiertes Exon 1B gefunden (Prowald et al. 2002b).
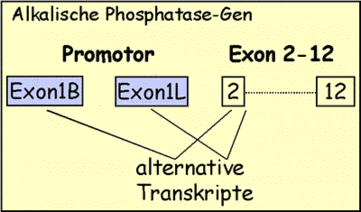
Abb. 1: Im Alkalische Phosphatase Transkript ist entweder Exon1L oder Exon1B enthalten. Exon2 bis einschließlich 12 unterscheiden sich nicht. Das Startcodon ist in Exon 2 enthalten, so dass sich die Proteine nicht in ihrer Aminosäuresequenz unterscheiden.
2. NF2 in Meningeomen
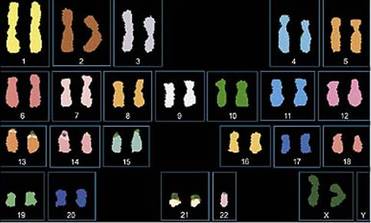
Wenige niedriggradige und die Mehrheit der hochgradigen Meningeome zeigen einen Verlust von Merlin, dem Genprodukt von NF2. NF2 steht für Neurofibromatose Typ 2. Das Gen ist auf Chromosom 22 lokalisiert. In Abbildung 2 ist ein entsprechendes Karyogramm gezeigt. Es handelt sich umeine SKY-Analyse (SKY steht für spectral karyotyping), bei der jedes einzelne Chromosom mit einer eigenen Fluoreszenzfarbe dargestellt werden kann.Merlin gehört zur Familie der 4.1 Proteine, die das Actin-Zytoskelett mit Zelloberflächenglykoproteinen verbinden. Ein weiteres Mitglied dieser Familie ist DAL-1, dessen Gen auf Chromosom 18 lokalisiert ist. DAL-1 steht für differentially expressed in adenocarcinoma of the lung. In 60 % der sporadischen Meningeome tritt ein Verlust von DAL-1 auf. Beide Proteine interagieren mit beta-Spectrin II. In einem Projekt wird die Expression dieser Gene in Meningeomen untersucht.
|
Abb. 2: Chromosom 22-Verlust in einem Meningeom. Nachweis mittels SKY-Analyse (Zang et al., 2001). Die Chromosomen sind hier in einer Falschfarben-Ansicht gezeigt.